اصول طراحی مهندسی ژن برای تولید مواد ارزشمند در مخمر
وقتی پای قرار دادن ژنها توی مخمر میاد وسط، تا این موجودات ریز بتونن دارو و بقیهی مواد بدردبخور رو بسازن، یه چیزی لازمه و اون اینه که بشه این تولید رو با اطمینان روشن و خاموش کرد. یه گروه از دانشگاه کُبِه سه تا اصل مهم توی طراحی ژن رو پیدا کردن که به ما یه نقشهی راه انعطافپذیر برای کنترل درست و حسابی تولید میکروبی میده.
میگن DNA نقشهی راه زندگیه و به سلولهامون میگه چی بسازن. اما DNA خودش یه سری کلید و دکمه هم داره که به این سلولها میگه کی چی بسازن و چقدر بسازن. برای همین، وقتی ژنهای جدید رو وارد سلولها میکنیم تا مواد شیمیایی مفید مثل دارو یا مواد اولیهی تولید شیمیایی رو بسازن، خیلی ضروریه که یه کلید ژنتیکی همراهشون باشه؛ یه تیکه از DNA که اسمش «پروموتر»ه. این پروموتر به سلولها میگه کی تولید رو شروع کنن.
ماساهیرو تو میناگا، مهندس زیستفناوری از دانشگاه کُبِه، میگه: «مسئله اینه که نمیشه این پروموترها رو همینطوری سرهم کرد و استفاده کرد، مگه اینکه محققها یه درک عمیق از نحوهی تعاملشون با بقیهی عناصر ژنتیکی داشته باشن. واقعیت اینه که الان خیلی کم پیش میاد که محققها از پروموترهای مصنوعی برای کنترل دقیق تولید سلولی و رسیدن به اهداف تحقیقاتیشون بتونن استفاده کنن.»

بعضی وقتا تولید خیلی کمه، و بعضی وقتا هم «نشت» داره، یعنی نمیشه هر وقت خواستیم خاموشش کنیم. این موضوع مخصوصاً توی مهندسی ژنتیک مخمر صدق میکنه، چون تنظیم ژنتیکش نسبت به باکتریها پیچیدهتره. اما این پیچیدگی بیشتر، در عین حال امکان تولید کلی مواد شیمیایی مفید رو فراهم میکنه.
تو میناگا و همکاراش که توی اصلاح سلولهای مخمر متخصص هستن، از تیم ایشی جون، یه رویکرد سیستماتیک برای طراحی پروموترهای مؤثر در نظر گرفتن. تو میناگا توضیح میده: «به این فکر رسیدیم که اگه بتونیم فرآیند بهبود یه پروموتر نمونه رو با جزئیات توضیح بدیم، میتونیم یه راهنمای کاربری درست کنیم که به ما کمک کنه به کنترل دقیق و بازدهی بالا برسیم، تا بشه از این سیستمهای ژنتیکی بیشتر استفاده کرد.»
اونا توی یه مقالهای که الان توی مجلهی Nature Communications چاپ شده، سه تا اصل طراحی برای پروموترهای مخمر رو توضیح دادن. اولین اصل اینه که اگه محققها به مقدار زیادی از محصول نیاز دارن و در عین حال میخوان بتونن تولید رو هر وقت خواستن روشن و خاموش کنن، باید چند تا کپی از عناصر تنظیمی که این کارو ممکن میکنن، توی پروموتر قرار بدن.
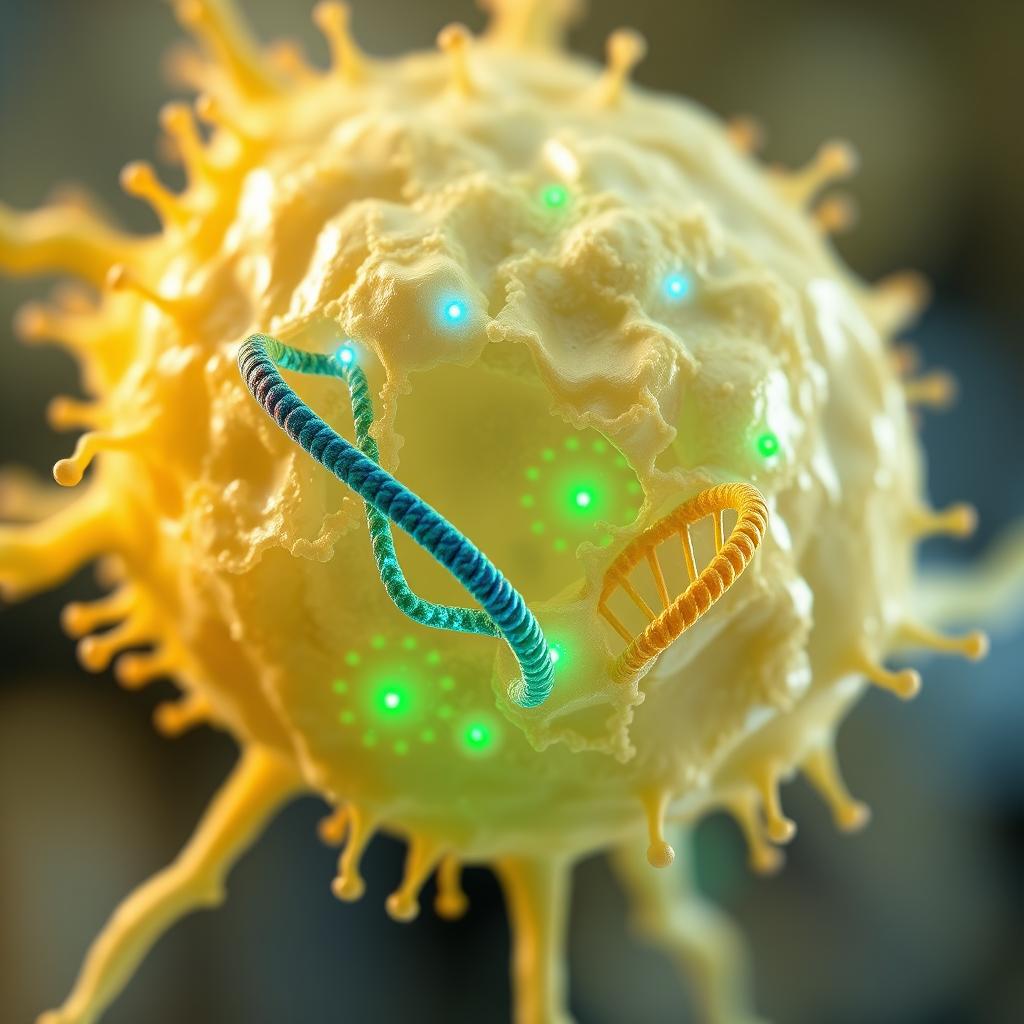
کم کردن نشت و بالا بردن راندمان توی پروتئینهای دارویی
این روش نشت رو کم میکنه و راندمان رو بالا میبره. نکتۀ دوم اینه که فاصلهی بین عناصر پروموتر باید تا جایی که میشه کم باشه تا راندمان بیشتر بشه. نکتۀ سوم اینه که پروموتر باید از DNA اطرافش جدا بشه، یعنی DNA اضافی قبل ازش قرار بگیره تا نشت رو باز هم کمتر کنه. تومینگا میگه: «ما نشون دادیم که عملکرد یه پروموتر میتونه با تغییر توالیهای اطرافش، بیشتر از ۱۰۰ برابر بهتر بشه. این اولین تحقیقیه که یه راهحل روشن برای این مشکل ارائه میده که چرا پروموترهای قوی توی مخمر، توی بعضی محیطها کار میکنن و توی بعضی دیگه نه.»
مهندسهای زیستی دانشگاه کُبِه، با نشون دادن تولید دو تا پروتئین دارویی مفید به اسم “بیولوژیکها“، تونستن کارآیی سیستم خودشون رو ثابت کنن. اونا نه تنها تونستن این دو تا بیولوژیک رو توی مخمرهای جداگانه تولید کنن، بلکه تونستن این کارو توی یه سویهی واحد و با قابلیت کنترل مستقل تولید هر بیولوژیک در هر زمان هم انجام بدن. این نکته خیلی مهمه، چون کاربردهای بالقوهی زیادی توی بیمارستانها داره. همونطور که تیم توی این مطالعه توضیح داده: «علاوه بر تخمیر معمولی بیولوژیکهای تکی، تولید سریع و دوز فوری چند تا بیولوژیک با یه سویهی مخمر توی محل درمان، برای موقعیتهای اورژانسی که سرعت و انعطافپذیری بیشتر از خلوص و راندمان لازمه، حیاتیه.»
اونا همچنین تونستن پروتئین کروناویروس رو تولید کنن که میشه ازش برای ساخت درمانها استفاده کرد. این موضوع نشون میده که اصول طراحیشون چقدر کارآمده و منعطفه. تومینگا یه دید وسیعتر دربارهی پیامدهای این مطالعه ارائه میده: «زیستشناسی سنتزی دنبال اینه که عملکردهای بیولوژیکی جدید رو از طریق بازنویسی توالیهای ژنومی ایجاد کنه. اما واقعیت اینه که ما معمولاً با تغییرات غیرمنتظرهای که از ویرایشهای خودمون ناشی میشه، گیج میشیم. امیدواریم که مطالعهی ما اولین قدم به سمت این باشه که بتونیم هر کدوم از پایههای ژنوم رو با یه هدف مشخص طراحی کنیم.»
این تحقیق با حمایت مالی سازمان تحقیقات و توسعهی پزشکی ژاپن (کمکهای مالی JP21ae0121002, JP21ae0121005, JP21ae0121006, JP21ae0121007, JP20ae0101055 و JP20ae0101060)، سازمان علم و فناوری ژاپن (کمکهای مالی JPMJCR21N2 و JPMJGX23B4) و انجمن پیشبرد علم ژاپن (کمکهای مالی JP23K26469, JP23H01776 و JP18K14374) انجام شده. این تحقیق با همکاری محققهای شرکت Pharma Foods International Co. Ltd و موسسه ملی علوم بهداشتی انجام شد.



بیشتر بخوانید
مدیتیشن یک روز پربرکت برای جذب عشق وامنیت و سلامتی
خود هیپنوتیزم درمان زود انزالی در مردان توسط هیپنوتراپیست رضا خدامهری
تقویت سیستم ایمنی بدن با خود هیپنوتیزم
شمس و طغری
خود هیپنوتیزم ماندن در رژیم لاغری و درمان قطعی چاقی کاملا علمی و ایمن
خود هیپنوتیزم تقویت اعتماد به نفس و عزت نفس