تحقیقات نوین پیرامون بیماری خودایمنی شوگرن
تحقیقاتی که توی دانشکده دندانپزشکی دانشگاه نیویورک و همچنین دانشکده پزشکی گروسمن همین دانشگاه انجام شده، یه درک عمیقتری از عوامل موثر توی بیماری خودایمنی شوگرن رو نشون میده. این پیشرفتها، مدیون کشفیات جدید در مورد نقش سیگنالدهی کلسیم، سلولهای T تنظیمی و اینترفرون هست. مطالعه اخیرشون که توی مجله Science Translational Medicine چاپ شده، نشون میده که اختلال توی سلولهای T تنظیمی، عامل مهمیه توی بروز بیماری شوگرن توی موشها و آدمها، و یه داروی موجود توی روماتولوژی رو به عنوان یه درمان امیدبخش برای این بیماری معرفی کرده.
بیماری شوگرن و اثراتش
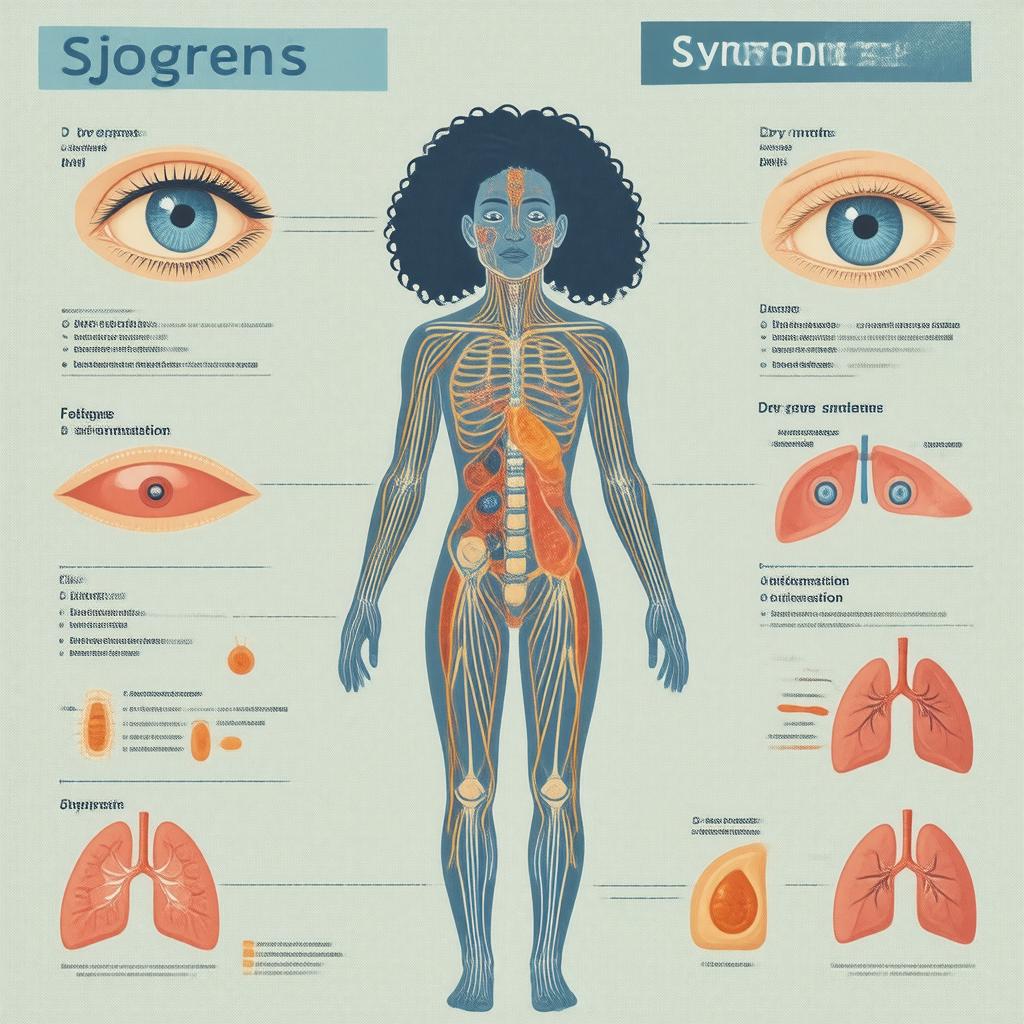
توی بیماری شوگرن، سیستم ایمنی به غدههایی که بزاق و اشک تولید میکنن حمله میکنه و نتیجهاش خشکی دهان و چشمها میشه. این بیماری میتونه روی بقیه قسمتهای بدن هم اثر بذاره و بعضی از بیماران ممکنه خستگی، درد توی مفاصل و عضلات، بثورات پوستی و التهاب ریه رو تجربه کنن. رودریگو لاکروز، استاد پاتوبیولوژی مولکولی توی دانشکده دندانپزشکی نیویورک، گفت: “ناتوانی توی تولید اشک یا بزاق میتونه تاثیر زیادی روی زندگی یه نفر بذاره. اگه نتونی بزاق تولید کنی، ممکنه روی صحبت کردن و تواناییات برای خوردن غذا تاثیر بذاره، احتمال پوسیدگی دندون رو زیاد کنه و کلا سلامت فرد رو به خطر بندازه.”
ویژگیهای بیماری شوگرن
علاوه بر کم شدن تولید اشک و بزاق، ویژگیهای بیماری شوگرن و عواملی که به پزشکا توی تشخیصش کمک میکنن شامل وجود آنتیبادیهای خودکار توی خون و لنفوسیتها توی غدد بزاقی میشه. در حال حاضر درمان قطعی برای بیماری شوگرن وجود نداره، اما بعضی درمانها علائم رو کم میکنن، هرچند که شاید نتونن بیمارا رو کاملا خوب کنن. استفان فسکه، استاد پزشکی توی دپارتمان پاتولوژی دانشگاه نیویورک، گفت: “بیماری شوگرن یه بیماری ناشی از التهابه. درمانهایی برای شوگرن هست که با آنتیبادیها سلولهای B رو از بین میبرن، اما نتایجشون توی آزمایشهای بالینی متفاوت بوده.”

تحقیقات در سطح سلولی
فسکه و لاکروز دو تا مطالعه روی بافتهای مختلف – سلولهای غدد بزاقی و سلولهای ایمنی – انجام دادن تا بهتر بفهمن که توی سطح سلولی چه اتفاقی میافته که بیماری شوگرن بروز میکنه. اونا به طور خاص، سلولهایی رو بررسی کردن که ژنهای Stim1 و Stim2 نداشتن، ژنهایی که سیگنالدهی کلسیم، یعنی مهمترین ماده معدنی بدن، رو مختل میکنن.
نقش سیگنالدهی کلسیم
لاکروز و فسکه روی نقش سیگنالدهی کلسیم توی بیماریهای انسانی، از جمله اختلالات سیستم ایمنی و بیماریهایی که روی دهان تاثیر میذارن، تحقیق کردن. سیگنالدهی کلسیم برای تولید بزاق خیلی مهمه، اما هنوز معلوم نیست که چقدر توی پیشرفت بیماری شوگرن نقش داره. توی یه مطالعه که اخیراً توی مجله Function منتشر شده، محققان موشهایی رو که ژنهای Stim1 و Stim2 رو توی سلولهای غدد بزاقی نداشتن، بررسی کردن. این نقص باعث شد که این سلولها کلسیم جذب نکنن. اونا فهمیدن که این موشها بزاق کمتری تولید میکردن که دلیلش کمبود کلسیم و سیگنالدهی بود. با این حال، این موشها التهاب غدد بزاقی یا زیاد شدن سطح آنتیبادیهای خودکار، که از علائم بیماری شوگرن توی آدمهاست، رو نداشتن. این نشون میده که کمبود سیگنالدهی کلسیم توی سلولهای غدد بزاقی، ممکنه در واقع پاسخهای التهابی رو سرکوب کنه، نه اینکه این موشها رو مستعد التهاب و آنتیبادیهای خودکار کنه.
لاکروز، که سرپرست این مطالعه توی Function بود، گفت: “ما فهمیدیم که یه کانال کلسیم خاص که توسط پروتئینهای STIM1 و STIM2 فعال میشه، برای ترشح بزاق ضروریه، که یه کشف مهمه. کمبود سیگنالهای کلسیم نه تنها عملکرد رو مختل میکنه، بلکه ممکنه اثر مولکولهای التهابی که با بیماری شوگرن در ارتباط هستن رو هم کم کنه.”
نقش سلولهای T تنظیمی
مطالعات قبلی نشون داده بودن که تغییر ژنتیکی موشها به طوری که سیگنالدهی کلسیم توی سلولهای T سیستم ایمنیشون مختل بشه، باعث اختلال توی یه نوع خاصی از سلولهای T – سلولهای T تنظیمی – میشه که التهاب و بیماری خودایمنی رو توی موشها به وجود میاره. سلولهای T تنظیمی به کنترل پاسخ سیستم ایمنی کمک میکنن، اما وقتی درست کار نکنن، نمیتونن جلوی بروز بیماری خودایمنی رو بگیرن.
تحقیقات جدید درباره سلولهای T تنظیمی و بیماری شوگرن
به خاطر نتایج ضد و نقیض تحقیقات قبلی درباره سلولهای T تنظیمی و بیماری شوگرن، این سلولها محور اصلی کارهای فِسکه و لاکِرز شدن. توی مطالعهای که توی Science Translational Medicine منتشر شد و فسکه رهبریش رو به عهده داشت، پژوهشگرا دوباره به بررسی موشهایی پرداختن که ژنهای Stim1 و Stim2 نداشتن و در نتیجه سیگنالهای کلسیم نداشتن. اما این بار، تمرکز روی سلولهای T تنظیمی بود، نه سلولهای غدد بزاقی.
اختلال توی سلولهای T تنظیمی باعث التهاب شدید توی موشها شد که با معیارهای تشخیص بیماری شوگرن همخوانی داشت: چشمهای خشک، دهان خشک، آنتیبادیهای خودایمنی و لنفوسیتها توی غدد بزاقی. بعضی از موشها هم دچار التهاب ریه شدن که میتونه نشونهای از بیماری شوگرن باشه. فسکه گفت: “حذف این دو تا ژن باعث ایجاد یه زنجیره از اختلالات ایمنی شد.” آیا سیگنالدهی مختل شده کلسیم، یه پاسخ خودایمنی مشابه بیماری شوگرن رو توی موشها تحریک کرده بود؟
توی بررسیهای بیشتر روی موشها و سلولهای خونی آدمها، پژوهشگرا نتیجه گرفتن که مشکل اصلی، اختلال توی سلولهای T تنظیمیه که میتونه از راههای مختلفی اتفاق بیفته، نه فقط سیگنالدهی کلسیم. یه عامل احتمالی که علائم بیماری شوگرن رو توی موشها ایجاد میکنه، اینترفرون گاما هست. فسکه گفت: “این موضوع مربوط به نقص توی سلولهای T تنظیمی و فعالیت زیاد سلولهایی میشه که یه سیتوکین التهابی به اسم اینترفرون گاما تولید میکنن. اینترفرون گاما برای ایجاد اختلال توی غدههای بزاقی توی مدل موشی ما کاملا حیاتی بود.”
سلولهای T تنظیمی معمولا از فعالیت بقیه سلولهای ایمنی، از جمله سلولهایی که اینترفرون گاما تولید میکنن، جلوگیری میکنن. حذف سیگنالدهی کلسیم توی سلولهای T تنظیمی، سلولهای تولیدکننده اینترفرون گاما رو آزاد کرد و بهشون اجازه داد که سیتوکین بیشتری تولید کنن. با این حال، وقتی پژوهشگرا اینترفرون گاما رو بهطور ژنتیکی از سلولهای T موشها حذف کردن، عملکرد غدههای بزاقی بهتر شد. آیا یه دارو میتونه همین کار رو بکنه؟
برای امتحان کردن این ایده، پژوهشگرا به یه داروی موجود به اسم باریسیتینیب روی آوردن که در حال حاضر برای درمان آرتریت روماتوئید، آلوپسی و اخیراً بیماران بستری مبتلا به COVID-19 استفاده میشه. باریسیتینیب یه مهارکننده JAK (Janus kinase) هست که با سرکوب سیگنالهای پاییندست گیرنده اینترفرون، التهاب رو کم میکنه. وقتی پژوهشگرا باریسیتینیب رو به موشها دادن، اختلال و التهاب غدههای بزاقی رو کنترل کرد. با توجه به موفقیت این دارو توی موشهایی که علائم شوگرن داشتن، چه توی این مطالعه و چه توی مطالعات دیگه، پژوهشگرا فکر میکنن که باریسیتینیب میتونه کاندیدای خوبی برای درمان بیماری شوگرن باشه.
برای این که مشخص بشه که آیا یافتههاشون توی موشها به آدمها هم میخوره یا نه، پژوهشگرا نمونههای خونی رو از بیماران مبتلا به بیماری شوگرن هم بررسی کردن. با استفاده از دنبالهنگاری RNA تکسلولی برای مطالعه سلولهای خونی سفید، اونا ارتباط قوی بین بیان ژن توی سلولهای موشها و آدمها با بیماری شوگرن پیدا کردن. فسکه گفت: “ما نه تنها علت اصلی بیماری شوگرن رو توی مدل موشیمون بررسی کردیم، بلکه این یافتهها رو با معیارهای تشخیص بیماری و امضای ژنتیکی توی آدمها مرتبط کردیم. علاوه بر این، فکر میکنم استفاده از باریسیتینیب توی درمان بیماری شوگرن توی آینده خیلی امیدوارکننده است.”
نویسندههای دیگه مطالعه Science Translational Medicine شامل یین-هو وانگ، وهی لی، مکدِرموت، فانگ ژو، آنتونی تائو، دیمیتریوس رافائل، آندره ال. موریرا، بوهنگ شن، جورج مایتی، مارتین وِت، بتینا نادورپ و شکتی چاکراورتی از دانشکده پزشکی NYU Grossman و گا-یون سون از دانشکده دندانپزشکی NYU هستن. این مطالعه توسط مؤسسات ملی بهداشت (R01DE027981، EY030917، U01DE028891، AI164803)، مرکز کولتون برای خودایمنی در NYU و پروژه تحقیقاتی و نوآوری دانشجویان تحصیلات تکمیلی استان هونان (CX20190160) از دانشگاه مرکزی و جنوبی چین حمایت شد. نویسندههای دیگه مطالعه Function شامل گا-یون سون و آنا زو از دانشکده دندانپزشکی NYU، آماندا وال، کای تینگ هوانگ، لری واگنر و دیوید آی. یول از دانشگاه راچستر و سارول زُرگیت، مانیکاندان وینو و یوسف ایداگدور از NYU ابوظبی هستن. این مطالعه همچنین توسط مؤسسات ملی بهداشت (R01DE027981، DE014756، U01DE028891، P30CA016087) حمایت شد.



بیشتر بخوانید
مدیتیشن یک روز پربرکت برای جذب عشق وامنیت و سلامتی
خود هیپنوتیزم درمان زود انزالی در مردان توسط هیپنوتراپیست رضا خدامهری
تقویت سیستم ایمنی بدن با خود هیپنوتیزم
شمس و طغری
خود هیپنوتیزم ماندن در رژیم لاغری و درمان قطعی چاقی کاملا علمی و ایمن
خود هیپنوتیزم تقویت اعتماد به نفس و عزت نفس