بررسی تومورهای کرانیوفارنژیوم: دریچهای به سوی درمانهای هدفمندتر
تومورهای کرانیوفارنژیوم، مزاحمهای کوچکی در مغز هستند که متاسفانه کارکرد هورمونی غدهی هیپوفیز، که مسئولیتهای مهمی داره، رو مختل میکنن. موقعیت این تومورها معمولاً کار جراحها رو سخت میکنه و مانع از عملهای حیاتی میشه. برای جایگزین کردن روشهای دارویی، باید ریزهکاریهای مولکولی این تومورها رو خوب بشناسیم. محققان ژاپنی با این هدف، به بررسی بیان ژن توی سلولهای توموری پرداختن. نتایج این تحقیق، اطلاعاتی در مورد ویژگیها و تعاملات مولکولی سلولهای توموری و سیستم ایمنی در دو نوع فرعی کرانیوفارنژیوم ارائه میده، که میتونه در پیدا کردن راههای درمان هدفمند در آینده خیلی کمک کنه.
ویژگیهای تومور کرانیوفارنژیوم
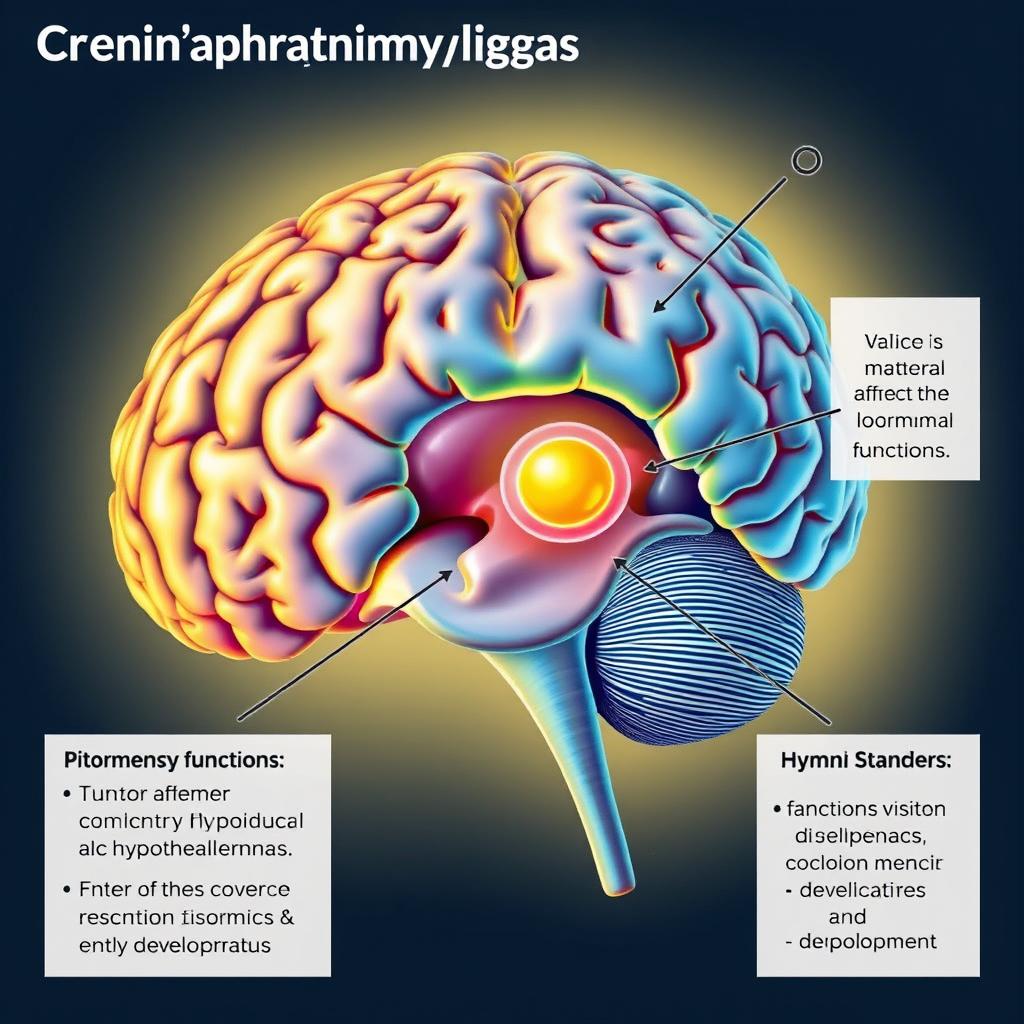
کرانیوفارنژیوم (CP) نوعی تومور نادر مغزیه که توی مناطق نزدیکی هیپوتالاموس و غدهی هیپوفیز به وجود میاد. این تومورها عوارضی مثل مشکلات بینایی، اختلالات عصبی، دیابت و مشکلات رشدی رو به دنبال دارن. دو نوع اصلی CP وجود داره: کرانیوفارنژیوم آدامانتینوماتوز (ACP) و کرانیوفارنژیوم پاپیلاری (PCP). این دو نوع با تفاوتهایی که در ژنهاشون هست، از هم متمایز میشن. معمولاً ACP با جهشهایی در ژن CTNNB1 شناخته میشه، در حالی که PCP بیشتر با جهش در ژن BRAF در ارتباطه.
چالشهای درمانی
متاسفانه، عمل جراحی راه اصلی درمان CP هست. اما ماهیت تهاجمی تومور و نزدیکی اون به ساختارهای حساس مغز، چالشهای بزرگی رو در جراحی ایجاد میکنه. با بزرگ شدن تومور، به بافتهای اطراف نفوذ میکنه و باعث مشکلات جدی عصبی میشه. به همین دلیل، فقط جراحی برای مقابله با مشکلات پیچیدهای که CP به وجود میاره، کافی نیست. برای اینکه بتونیم تومور رو با موفقیت خارج کنیم و در عین حال بافتهای سالم اطراف رو حفظ کنیم، باید اطلاعات کاملی از ویژگیهای زیستی و پیشرفت مولکولی تومور داشته باشیم.
همکاری محققان برای بررسی زیستشناسی تومور
پروفسور توموآکی تاناکا با همکاری پروفسور یوشینوری هیگوچی و دکتر تاکاشی کونو از دانشکدهی پزشکی دانشگاه چیبا در ژاپن، مطالعهای رو برای روشن کردن فرایندهای زیستی زیربنایی این تومور انجام دادن. این مطالعه در تاریخ ۳۰ سپتامبر ۲۰۲۴ به صورت آنلاین منتشر شد و در شماره ۱۱ مجله iScience در ۱۵ نوامبر ۲۰۲۴ به چاپ رسید. برای این کار، از روش توالییابی RNA تکسلولی استفاده کردن، که تفاوتهای بیان ژن رو توی تکتک سلولها نشون میده و اطلاعاتی در مورد ۱۰ مورد CP به دست آوردن. پروفسور تاناکا، که سرپرست این تحقیق بود، در یک مصاحبه انگیزههای پشت این تحقیق رو توضیح داد.
تحلیل تأثیر تومورهای خوشخیم بر ساختارهای حیاتی مغز
ایشون گفت: “با وجود اینکه این تومورها از نظر بافتی خوشخیم هستن، اما میتونن تاثیرات قابل توجهی روی ساختارهای حیاتی مغز داشته باشن.” و اضافه کرد: “هدف ما، توسعهی روشهای درمانی هدفمند و کم تهاجمه که بتونن به طور قابل توجهی نتایج بیماران و کیفیت زندگیشون رو بهتر کنن.“
تحلیل تکسلولی و تنوع در محیط میکروتومور
تحلیل تکسلولی نشون داد که توی محیط میکروتومور (TME)، انواع مختلفی از سلولها وجود داره، از جمله سلولهای توموری، سلولهای ایمنی و فیبروبلاستها، که نسبتهاشون در بیماران مختلف فرق میکرد. سلولهای توموری به دو زیرگروه اصلی تقسیم شدن: نوع ۱ که بیشتر توی ACP دیده میشه و نوع ۲ که توی PCP غالب هست. اطلاعات به دست اومده از بیان ژن سلولهای تکسلولی، زیرگروههای ACP و PCP رو از هم جدا کرد و انواع مختلف سلولهای داخل تومور رو مشخص کرد.
شناسایی انواع سلولهای مرتبط با تومورها
این تحقیق سلولهایی رو شناسایی کرد که با رشد سلولهای اپیتلیال و پاسخ ایمنی در تومورهای ACP و PCP مرتبط بودن. اما سلولهایی که توی کلسفیکاسیون تومور نقش داشتن، بیشتر توی ACP دیده میشدن، در حالی که ژنهای مرتبط با چرخه سلولی توی PCP غالب بودن. علاوه بر این، تیم تحقیقاتی تنوع قابل توجهی رو توی انواع ماکروفاژها بین دو نوع تومور مشاهده کرد. ماکروفاژهای M1 که التهاب رو افزایش میدن و نشانگرهای التهابی، توی ACP بیشتر بودن، در حالی که ماکروفاژهای M2 که ضد التهابی هستن، توی PCP بیشتر دیده میشدن. به همین ترتیب، نسبت بالاتر ماکروفاژهای M1 و M2 با بروز دیابت و نارسایی هیپوفیز مرتبط بود.
تعاملات سلولی و سیگنالدهی در تومورها
علاوه بر این، مطالعه نشون داد که تعامل مهمی بین پروتئینهای CD44 و فسفروپروتئین 1 (SPP1) وجود داره. این سیگنال SPP1-CD44 از ماکروفاژهای کلاسیک M2، رشد سلولهای T رو متوقف میکنه. این مطالعه، نقشهی کاملی از انواع سلولها در تومورهای CP ارائه میده و ارتباط مهمی بین سلولهای ایمنی و علائم بالینی رو نشون میده.

پیامدهای بالینی و آینده درمانهای هدفمند
پروفسور تاناکا به اهمیت یافتههاش توی درمان بیماران اشاره کرد و گفت: “این یافتهها امکان درمانهای شخصیسازی شده رو برای بیماران مبتلا به CP فراهم میکنه، بر اساس نوع تومور و ترکیب سلولهای ایمنیشون.” ایشون اضافه کرد: “درک این تفاوتها به پزشکها کمک میکنه تا پیشبینی کنن کدوم بیماران بیشتر در معرض عوارضی مثل دیابت بیمزه هستن.
“”
با پیشرفت این یافتهها، میشه به درمانهای هدفمند جدیدی دست پیدا کرد که مستقیماً روی محیط میکروتومور و تعاملات سلولهای ایمنی تاثیر بذاره و در نهایت، درمانهای موثرتری با عوارض جانبی کمتر به دست بیاد.





بیشتر بخوانید
مدیتیشن یک روز پربرکت برای جذب عشق وامنیت و سلامتی
خود هیپنوتیزم درمان زود انزالی در مردان توسط هیپنوتراپیست رضا خدامهری
تقویت سیستم ایمنی بدن با خود هیپنوتیزم
شمس و طغری
خود هیپنوتیزم ماندن در رژیم لاغری و درمان قطعی چاقی کاملا علمی و ایمن
خود هیپنوتیزم تقویت اعتماد به نفس و عزت نفس